
原标题:PD-1/PD-L1免疫医治系列:Imfinzi最新获批一线医治小细胞肺癌!
Imfinzi,俗称I药(别的有O药Opdivo、K药Keytruda,T药Tecentriq),各个免疫制剂各有千秋。PD-1包含:K药和O药;PD-L1包含T药和I药。
近来,I药又获批最新适应症,本文详做介绍。
2020年3月30日,美国FDA同意阿斯利康研发出产的PD-L1抗体Imfinzi (durvalumab,德瓦鲁单抗)联合化疗(依托泊苷+卡铂/顺铂)用于医治未经体系医治的广泛期小细胞肺癌(ES-SCLC)患者的一线医治。
小细胞肺癌(SCLC)是一种侵略性,增长速度极快的肺癌。一般分为两个阶段:有限阶段和广泛阶段性疾病。约有三分之二的患者在初诊疾病已发展到广泛期。
商品名:Imfinzi(英飞凡)
通用名:durvalumab(德瓦鲁单抗)
厂家:阿斯利康
标准:500 mg/10mL或120 mg/2.4mL
初次获批时刻:2017年5月
小细胞肺癌引荐剂量:1500mg联合化疗,每3周(21天),共4个周期,之后调整剂量每4周1500mg
CASPIAN是一项随机,敞开标签,全球,多中心的III期临床实验研讨,实验旨在研讨I药联合化疗一线医治广泛期小细胞肺癌患者的安全性和效果性。契合条件的患者WHO状况为0或1。
共招募537名患者,一切患者随机按1:1份额分配至I药+EP医治组268名or独自EP医治组269名。其间联合组医治直至疾病发展或不行承受的毒性;独自医治组医治6个周期后承受全脑预防性放射医治(PCI)。
实验首要研讨结尾为总生存期(OS),非必须研讨结尾为无发展生存期(PFS),客观缓解率(ORR)。
患者基线特征:中位年纪63岁(28—82岁),40%的患者年纪在65岁以上;70%男性;84%白人,15%亚洲人,0.9%黑人;65%以上ECOG/WHO评分为1,;93%为吸烟者;90%的患者为IV期;10%的患者在基线时有脑搬运;25%的患者承受了顺铂医治;74%承受卡铂医治。
实验成果显现,联合组与独自医治组中位OS为13个月 VS 10.3个月;中位PFS为5.1个月 VS 5.4个月;ORR(肿瘤缩小率)为68% VS 58%;12个月ORR为22.7% VS 6.3%。
图注:CASPIAN实验成果图
与独自化疗比较,I药联合化疗可将逝世危险下降27%。
在安全性方面,I药+EP医治组常见不良反应为厌恶(34%)、疲惫(32%)、掉发(31%)、胃口下降(18%)、便秘(17%)、咳嗽(15%)、吐逆(15%)、皮疹(11%)、腹泻(10%)、甲状腺功用减退(10%)。
图注:CASPIAN实验不良反应图
【重要提示】本公号【医诺全球】文章信息仅供参考,详细医治谨遵医嘱!
责任编辑:

 万众瞩目:络病大会召开 微血管病变防治开辟新局面
万众瞩目:络病大会召开 微血管病变防治开辟新局面 毓婷x学院奖云课堂完美收官|“毓”青春同行,创意步履不“婷”
毓婷x学院奖云课堂完美收官|“毓”青春同行,创意步履不“婷”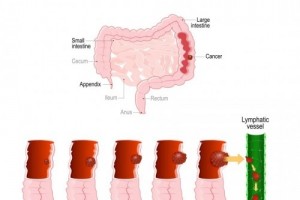 发现就是中晚期的结直肠癌,其实有办法可以避免!
发现就是中晚期的结直肠癌,其实有办法可以避免! “毓”见别YOUNG青春——毓婷携手学院奖2022再启新程
“毓”见别YOUNG青春——毓婷携手学院奖2022再启新程 成都中德肾病医院付冬梅--专业经验技术 让你放心无忧
成都中德肾病医院付冬梅--专业经验技术 让你放心无忧 成都中德肾病医院专家韩艳简介
成都中德肾病医院专家韩艳简介 屈燧林--成都中德肾病医院特聘专家
屈燧林--成都中德肾病医院特聘专家 成都中德肾病医院付冬梅主任:糖尿病肾病应该如何治疗与调养
成都中德肾病医院付冬梅主任:糖尿病肾病应该如何治疗与调养